彦根藩の当主である井伊直孝公をお寺の門前で手招き雷雨から救った
と伝えられる招き猫と井伊軍団のシンボルとも言える赤備え(戦国時
代の井伊軍団編成の一種、あらゆる武具を朱りにした部隊編成のこと
兜(かぶと)を合体させて生まれたキャラクタ-
【季語と短歌:4月24日】
地撒き跡 にわか花守 覗き込む 
高山 宇 大豆は茹でないで!
大豆は茹でないで!
なぜ?!大豆は茹でてしまうとせっかくの豊富な栄養が
流出してしまうから。どの程度 ロス?
血圧を正常に保つ作用のあるカリウムが約1.5倍
筋肉の動きをスムーズにし、体内の酵素を働きを支えるマグネシウムは…約1.6倍
出血したときに血液を固めるビタミンKは…約1.6倍
髪や肌の健康を保つビタミンB2は…約1.3倍
発育を促す葉酸は…約2.3倍
蒸すとロス少ない!

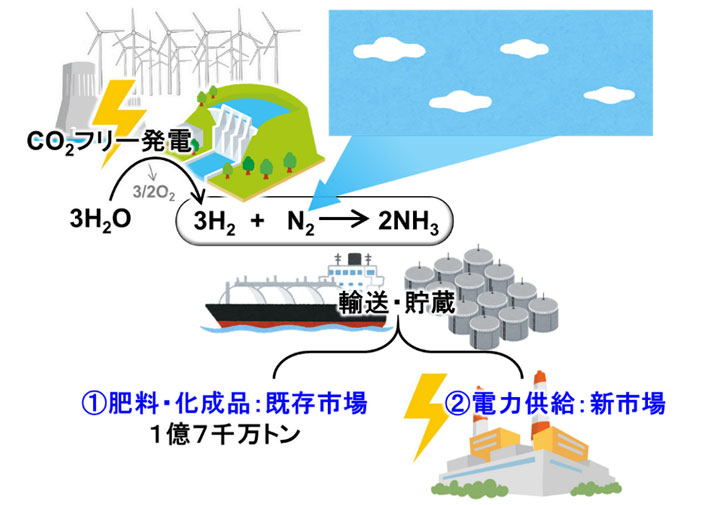
✳️ エネルギー資源としての水素とは
水素ガスは液化すると800分の1に体積が小さくなる一方、ボンベや
トレーラーで流通している高圧水素ガスは15~20MPa程度の圧力で約
150~200分の1に圧縮されている。このため、液化水素にすれば同じ
容量の容器に圧縮水素の4倍以上の量を計算上充填できることになる。
また実際の輸送では、高圧水素トレーラー1回当たりの輸送量が約
3,000N㎥であるのに対し、液化水素では最大12倍の3.6万N㎥を一度
に運んで貯蔵することが可能。これは、気体の場合は細長い重いボン
ベを束ねているため、どうしても充填量が少なくなる等の理由による。
このように、液化水素は大量輸送・大量貯蔵が容易なため、ユーザー
にとっては受入頻度の大幅削減・安定供給・省スペースなどのメリッ
トにつながる。
かつて産業用水素の大半は圧縮ガスで流通し、液化水素は宇宙ロケッ
トなど限られた用途のみに使われていたが、2006年に大阪府堺市に液
化水素製造プラント・ハイドロエッジを稼働して以来、液化水素の需
要は着実に増加。また水素は、ヘリウムに次いで沸点が低く-253℃
の極低温で液化する。そのため、水素を液化するときは、水素中の不
純物を取り除いておかないと、水素が-253℃になる過程で、ヘリウ
ム以外の不純物は固化してしまい、製造設備内で閉塞を引き起こすこ
とになる。したがって、液化水素は99.9999%以上の純度となっている。
こうしたことから水素を大量に消費するガラスや金属加工、高純度水
素へのニーズが高い半導体製造、電子部品、自動車関連などの産業分
野で、構内に液化水素のタンクを設置し、利用するユーザーが増えて
いる。「ガスは進化すると液体になる」。ここでいう進化とは、需要が
増し用途が広がって、大量消費されるという意味で、将来の本格的な
水素エネルギー時代には、水素も液化水素が主役になる。
1️⃣ 特願平03-069310 スラッシュ水素製造装置 岩谷産業株式会社
【特許請求の範囲】
【請求項1】 断熱密閉容器(1)内に収容した液体水素を凍結-融
解を繰り返すことによりスラッシュ水素を製造する装置であって、断
熱密閉容器(1)の下部に液体水素給排路(2)を接続するとともに、
断熱密閉容器(1)の上部に排気路(4)とヘリウムガス供給路(5)
とを接続し、排気路(4)に熱交換器(7)と真空ポンプ(9)とを
断熱密閉容器(1)側から順に配置し、断熱密閉容器(1)内に撹拌
手段(16)を配置し、この撹拌手段(16)を断熱密閉容器(1)
外から駆動可能に構成したスラッシュ水素製造装置。
【発明の詳細な説明】【0001】
【産業上の利用分野】本発明は、固体水素と液体水素とが共存してい
るスラッシュ水素を製造する装置に関する。
【従来技術】従来、スラッシュ水素を製造する原理としては、ジャケ
ット内に液体ヘリウムを流し、内壁に固体水素を氷結させ、スクリュ
ーにより壁面の固体水素を掻き落とす間接冷却法、低温のガス状ヘリ
ウムを液体水素内に吹き込んでヘリウム導入管の先端に固体水素を生
成する直接冷却法、密閉容器内に液体水素を入れ、密閉容器内を三重
点以下の圧力に減圧して液表面部分に固体層を発生させる連続減圧法、
密閉容器内を三重点以下の圧力に減圧して液表面に固体層を発生させ
たのち、密閉容器の内圧を三重点以上の圧力にすることにより、表面
固体層の容器壁面との接触部分を融解させて液内に沈降させる断続減
圧法等が知られているが、効率よくスラッシュ水素を製造する装置は
いまだ開発されていない。
【発明が解決しようとする課題】
間接冷却法によるスラッシュ水素の製造では、固体水素を生成する内
壁とスクリューとのクリアランス設定が微妙で、固体粒子径の均一化
が困難であるという問題があった。また、直接冷却法によるスラッシ
ュ水素の製造では、ヘリウム導入管の先端に形成される固体水素がガ
ス状ヘリウムの流れに沿って筒状に成長することから、撹拌により固
体水素を粉砕する必要があり、この場合でも固体粒子径の均一化が困
難であるという問題がある。【0004】
連続減圧法によるスラッシュ水素の製造では、液層の表面及び容器内
周壁と接触している部分から氷結することから、撹拌を行っても固体
層が破砕されにくく内部をスラッシュ状に形成するのが困難であると
いう問題がある。一方、断続減圧法では、減圧により一旦氷結した固
体を真空度を落とすことにより、容器周壁部分で融解し、液表面に形
成された固体層を液中に沈降させ、一定時間(数秒~十数秒)毎に液
体表面を気相に露出させて固体層の発生を成長を促進することができ
るが、この場合、固体粒子径を均一化することが困難であるうえ、大
型化が困難であるという問題があった。本発明は、このような点に着
目してなされたものであり、固体粒子径の整ったスラッシュ水素を効
率よく製造することのできる製造装置を提供することを目的とする。
【課題を解決するための手段】上述の目的を達成するために、本発明
は、断続減圧法でのスラッシュ水素製造装置において、断熱密閉容器
の下部に液体水素給排路を接続するとともに、断熱密閉容器の上部に
排気路とヘリウムガス供給路とを接続し、排気路に熱交換器と真空ポ
ンプとを断熱密閉容器側から順に配置し、断熱密閉容器内に撹拌手段
を配置し、この撹拌手段を断熱密閉容器外から駆動可能に構成したこ
とを特徴としている。【0006】
【作用】本発明では、断続減圧法でのスラッシュ水素製造装置におい
て、断熱密閉容器の下部に液体水素給排路を接続するとともに、断熱
密閉容器の上部に排気路とヘリウムガス供給路とを接続し、排気路に
熱交換器と真空ポンプとを断熱密閉容器側から順に配置し、断熱密閉
容器内に撹拌手段を配置し、この撹拌手段を断熱密閉容器外から駆動
可能に構成しているので、真空度を落として固体層を沈降させた際に、
撹拌手段による撹拌で固体を破砕して固体の粒子径を均一化して液体
に混合させることになる。この結果、流動性に優れたスラッシュ水素
を形成することができる。また、撹拌手段で固液混合を行うことから、
大きな内径の断熱密閉容器内で確実に氷結させることができるから、
スラッシュ水素の製造効率を高め、短時間で大量のスラッシュ水素を
形成することができることになる。【0007】
【実施例】図1は本発明装置の概略構成図を示し、図2は断熱密閉容
器の断面図である。図において、符号(1)は断熱密閉容器であり、
この断熱密閉容器(1)に液体水素を収容し、断熱密閉容器(1)内
の圧力を水素の三重点圧力(7 kPa)付近で上下させることによ
り断熱密閉容器(1)内にスラッシュ水素を製造するようにしてある。
【0008】断熱密閉容器(1)の下部には液体水素を断熱密閉容器
(1)内に供給するとともに、形成されたスラッシュ水素を排出する
液体水素給排路(2)が接続してあり、この液体水素給排路(2)に
液体水素充填取出弁(3)が配置してある。また、断熱密閉容器(1)
の上部には断熱密閉容器(1)内のガスを排出する排気路(4)と断
熱密閉容器(1)内に加圧用ヘリウムガスを供給するヘリウムガス供
給路(5)が接続してある。
排気路(4)には断熱密閉容器(1)側から開閉切換弁(6)、熱交換
器(7)、流量調整弁(8)、真空ポンプ(9)が配置してあり、ヘリ
ウムガス供給路(5)には流量調整弁(10)と流路開閉弁(11)
がヘリウムガス供給源(図示略)側から順に配置してある。
【0009】断熱密閉容器(1)は図2に示すように、2重槽に形成
してあり、内槽(12)と外槽(13)との間は真空断熱するととも
に、内外槽間の温度差を小さくするために内外槽間の空間に外槽冷却
用の液体窒素貯蔵槽(14)が配置してある。そして、内外各槽(12)
(13)には覗き窓(15)がそれぞれ形成してあり、この覗き窓(
15)が内槽(12)内の液体水素の状態を視認できるようにしてあ
る。また、内槽(12)の内部に撹拌手段(16)を配置し、この撹
拌手段(16)の回転軸(17)を断熱密閉容器(1)の上部開口(
18)外に配置した駆動モータ(19)で回転駆動させるように構成
してある。そして、この撹拌手段(16)の回転軸(17)と駆動モ
ータ(19)の出力軸とは磁性体を使用したカップリング装置(20
により非接触状態で回転伝動可能に構成してある。
【0010】2重槽で構成した断熱密閉容器(1)の内槽(12)内
には、収容されている液体水素内に突入する状態に熱電対で形成した
温度検出具(21)と密度測定具(22)とが配置してある。なお、
図中符号(23)は温度検出具(21)や密度測定具(22)の出力
信号を処理する制御装置、(24)は覗き窓(15)に対応させて配置
したビデオカメラであり、このビデオカメラ(24)により、液体水
素の状態をモニタできるようにしてある。また、断熱密閉容器(1
)の下部に配管されている液体水素の給排路(2)は断熱処理が施さ
れている。【0011】
次に、このスラッシュ水素製造装置を使用してのスラッシュ水素の製
造手順を説明する。十分に予冷した断熱密閉容器(1)内に液体水素
給排路(2)から液体水素を供給する。この場合、断熱密閉容器(1)
内は大気圧であることから、液体水素温度は20.3K、断熱密閉容
器内の圧力は101.4 kPa、液体水素の密度は70.81kg
/m3である。そして、排気路(4)を開通させて真空ポンプ(9)
を作動させ、断熱密閉容器(1)内の水素ガスを排出することにより、
断熱密閉容器(1)内を水素の三重点圧力である7.3 kPaまで
減圧する。これにより、液体水素の液表面部分及び内槽(12)の器
壁と接触している部分から氷結を開始する。このとき、液体水素の温
度は13.8K、密度は77.06kg/m3、固体水素の温度は13
.8K、密度は86.67kg/m3である。【0012】
そして、減圧後一定時間(10秒前後)が経過すると、排気路(4)
の開閉切換弁(6)を閉弁し、断熱密閉容器(1)内の内圧をわずか
に高めることにより、容器内の圧力は三重点圧力よりも高くなるから
氷結した水素は器壁からの入熱の影響をうけてその器壁と接触してい
る部分から融解剥離し、液表面部分で氷結している固体水素はそのま
ま液体水素中に沈降する。このとき、断熱密閉容器(1)内は撹拌手
段(16)で撹拌されていることから、氷結している固体水素が破砕
され、小さな固体水素として液体水素中に混合される。【0013】
真空度を落としてから一定時間(10秒前後)が経過すると、再び排
気路(4)の開閉切換弁(6)を開弁し、断熱密閉容器(1)から排
気して断熱密閉容器(1)内を三重点圧力まで減圧して、液体水素の
表面部分に固体水素を形成する。このような操作を繰り返して、覗き
窓(15)からの目視結果あるいは、断熱密閉容器(1)内で液体水
素中に突入配置した密度測定具(22)で検出した液体水素密度が三
重点温度での液体水素密度(77.06kg/m3)と三重点温度で
の固体水素密度(86.67kg/m3)との中間値(例えば、81.
54kg/m3)になると、断熱密閉容器(1)内の圧力を三重点圧
力に維持したまま数時間放置する。ここで数時間放置するのは、生成
直後の固体水素粒子はつのが突出した形状であることから流動性を阻
害するが、生成後数時間経過した固体水素粒子はつのが取れた形状に
なって流動性を阻害しない形状に変化するからである。
【0014】一定の放置時間経過後、ヘリウムガス供給路(5)の流
量調整弁(10)を開弁するとともに、液体水素給排路(5)の液体
水素充填取出弁(3)を開弁して、密閉断熱容器(1)内に加圧用の
ヘリウムガスを注入し、密閉断熱容器内(1)からたシャーベット状
のいわゆるスラッシュ水素を取り出す。【0015】
【発明の効果】本発明では、断続減圧法でのスラッシュ水素製造装置
において、断熱密閉容器の下部に液体水素給排路を接続するとともに、
断熱密閉容器の上部に排気路とヘリウムガス供給路とを接続し、排気
路に熱交換器と真空ポンプとを断熱密閉容器側から順に配置し、断熱
密閉容器内に撹拌手段を配置し、この撹拌手段を断熱密閉容器外から
駆動可能に構成しているので、真空度を落として固体層を沈降させた
際に、撹拌手段による撹拌で固体を破砕して固体の粒子径を均一化し
て液体に混合させることができ、流動性に優れたスラッシュ水素を形
成することができる。また、撹拌手段で固液混合を行うことから、大
きな内径の断熱密閉容器内での固体粒子の混合を均一化して氷結時の
核を形成することができ、固体粒子の生成速度を速めてスラッシュ水
素の製造効率を高め、短時間で大量のスラッシュ水素を形成すること
ができることになる。
【図面の簡単な説明】
【図1】本発明装置の概略構成図である。
【図2】断熱密閉容器の断面図である。
【符号の説明】
1…断熱密閉容器、 2…液体水素給排路、4…排気路、 5…ヘリウ
ムガス供給路、7…熱交換器、 9…真空ポンプ、16…撹拌手段。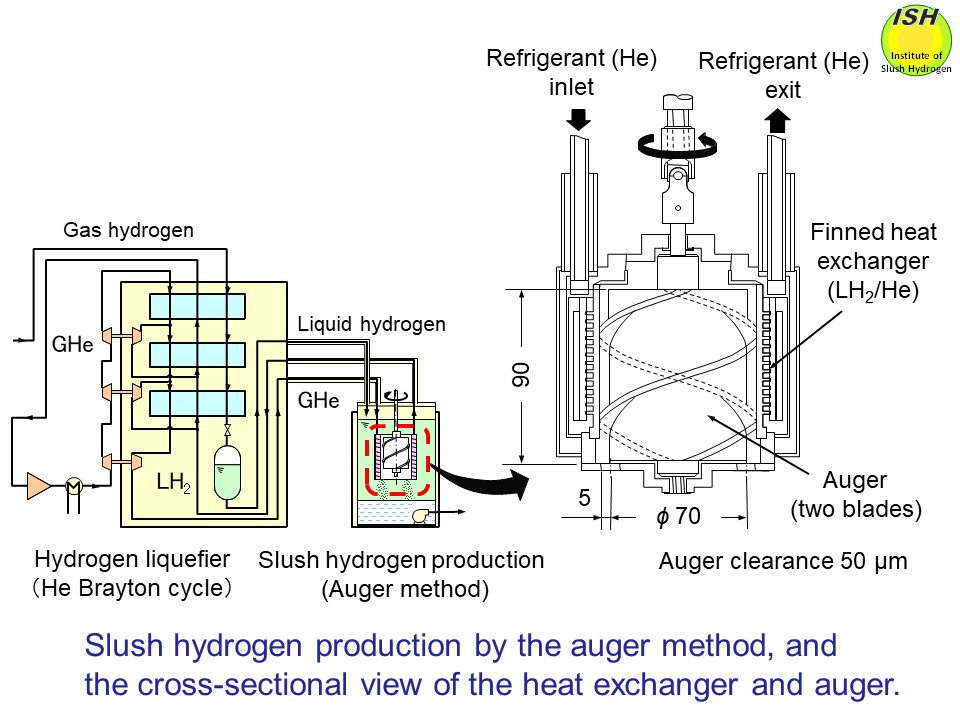
スラッシュ水素(スラッシュすいそ、Slush hydrogen)は、液体水素
よりも低温高密度で、液体水素と固体水素が入り混じった、水素の三
重点における状態である。液体水素を水素の融点(-259.14℃)付近
まで冷却することで得られる。この温度では、液体水素と比べ、密度
が16-20%大きくなる[1]。タンク容量を減らし、ロケットの重量を削
減できるため、液体水素の代替としてロケット燃料に用いることが提
案されている[2]。via Wikipedia (Hydrogen infrastructure)
液体水素:液体水素(えきたいすいそ)とは、液化した水素のこと。
沸点は-252.6℃で融点は-259.2℃である(重水素では、沸点-249.4℃)。
水素の液化は、1896年にイギリスのジェイムズ・デュワーが初めて成
功した。
水素燃料の課題:
製造 水素はもっとも軽い元素であり、地上において水素単体の形で
はほとんど存在していない。このため、エネルギー資源として水素を
直接採取・利用することはできず、必要な量はすべて水素化合物から
エネルギーを使って取り出さなければならない。最も身近な水素化合
物は水である。水を電気分解することで技術的には容易に水素が得ら
れるが、電気分解に消費される電気エネルギーは得られた水素を反応
させて再び得られる電気エネルギーより大きいために差し引きでは損
となる。エタノールや石油精製品から水素を取り出す方法もあるが、
その手間とコストを考えれば、そのままエタノールや石油精製品を燃
料として使用するほうが経済的である。いまのところ水素は天然ガス
と水より触媒を介する水蒸気改質で作り出されている。
保管:水素原子や水素分子は非常に小さいことから、金属の内部に浸
透して劣化させる水素脆化を引き起こす。そのためステンレスなどの
一般的な金属容器では長期保管が困難である。そこで、水素脆化が起
きない材料、水素を吸蔵する水素吸蔵合金、高圧水素用のCFRPボンベ、
冷却して液化水素として運搬・保管する方法などに関する研究開発が
進んでいる。
オルト水素とパラ水素:水素分子は、それぞれの原子核(プロトン)
の核スピンの配向により、オルト(ortho)とパラ(para)の2種類
の異性体が存在する[5]。常温以上では、オルト水素とパラ水素の存在
比はおよそ3:1であるが、低温になるほどパラ水素の存在比が増し、絶
対零度付近ではほぼ100パーセントパラ水素となる[5][6]。オルト水素
からパラ水素への変化は523kJ/kgの発熱反応であり、蒸発潜熱446kJ/
kgより多い。[7]また反応には数日かかるため、数日保管しておくと反
応熱で液化水素が気化してしまう。これを水素のボイル・オフ問題と
いう。[8]これを防止するには触媒を用いて発熱反応を済ませておくと
良い。オルト‐パラ変換を起こす触媒は、活性炭や鉄などの金属の一部、
常磁性物質またはイオンなどがある[5]。パラ水素をオルト水素に戻す
には、1週間近く常温で放置するか、触媒を用いるか、800℃ 近くに
加熱するとよい。[9] 以上
✳️ 貯蔵
2️⃣ 特開2025-40820 水素吸蔵システム及び水素吸蔵システムを備え
た水素エネルギーシステム 鹿島建設株式会社
【要約】下図2のごとく、水素吸蔵システム1は、水素を吸蔵する水
素吸蔵合金40Aを内部に収容する第1領域10Aと、水素を吸蔵す
る水素吸蔵合金40Bを内部に収容する第2領域10Bと、第1領域
10A及び第2領域10Bに収容された水素吸蔵合金40A,40B
の温度をそれぞれ調整する温度調整装置と、を備え、第1領域10A
と第2領域10Bとは、少なくとも一部が伝熱可能な隔壁11によっ
て区画されている。水素吸蔵システム1は、水素を吸蔵する水素吸蔵
合金40Aを内部に収容する第1領域10Aと、水素を吸蔵する水素
吸蔵合金40Bを内部に収容する第2領域10Bと、第1領域10A
及び第2領域10Bに収容された水素吸蔵合金40A,40Bの温度
をそれぞれ調整する温度調整装置と、を備え、第1領域10Aと第2
領域10Bとは、少なくとも一部が伝熱可能な隔壁11によって区画
されている。
図2、本発明の実施形態に係る水素吸蔵システムの概略図
図1、図1は、本発明の実施形態に係る水素吸蔵システムが適用され
る水素エネルギーシステムの概略図
【符号の説明】【0068】1・・・水素吸蔵システム2・・・水素発
生装置 3・・・水素利用装置 10・・・水素貯蔵タンク 10A
・・・第1領域 10B・・・第2領域11・・・隔壁(伝熱部)
20・冷却装置(温度調整装置)30・加熱装置(温度調整装置)
40A・・・水素吸蔵合金 40B・・・水素吸蔵合金
50A・・・第1循環回路 50B・・・第2循環回路
100・・・水素エネルギーシステム
【発明の効果】
水素吸蔵合金による水素の吸着あるいは脱着時において生じる熱エネ
ルギーを有効に利用できる。
【特許請求の範囲】
【請求項1】
水素を吸蔵する水素吸蔵合金を内部に収容する第1領域と、
水素を吸蔵する水素吸蔵合金を内部に収容する第2領域と、
前記第1領域及び前記第2領域に収容された前記水素吸蔵合金の温
度をそれぞれ調整する温度調整装置と、を備え、
前記第1領域と前記第2領域とは、少なくとも一部が伝熱可能な伝
熱部によって区画されている水素吸蔵システム。
【請求項2】
請求項1に記載された水素吸蔵システムであって、
前記第1領域は、全体が前記第2領域の内部に収容されている水素吸
蔵システム。
【請求項3】
請求項1に記載された水素吸蔵システムであって、
前記第1領域及び前記第2領域が、交互に配置された水素吸蔵システム。
【請求項4】
請求項1に記載された水素吸蔵システムであって、
前記第1領域及び前記第2領域の一方に収容された前記水素吸蔵合
金が水素を吸着した際に発生した熱によって、前記第1領域及び前記
第2領域の他方に収容された前記水素吸蔵合金を前記伝熱部を通じて
加熱する水素吸蔵システム。
【請求項5】
請求項1に記載の水素吸蔵システムであって、
前記第1領域において水素を吸着しているときに前記第2領域から
水素を脱着させるとともに、前記第2領域において水素を吸着してい
るときに前記第1領域から水素を脱着させ、これらを交互に繰り返し
行う水素吸蔵システム。
【請求項6】
請求項1から5のいずれか1つに記載の水素吸蔵システムと、
前記水素吸蔵システムに水素を供給する水素発生装置と、
前記水素吸蔵システムから放出された水素を利用する水素利用装置と、
を備え、前記水素発生装置から供給された水素を前記水素吸蔵システ
ムの前記第1領域または前記第2領域のいずれか一方に吸蔵させるの
と同時に、前記水素吸蔵システムの前記第1領域または前記第2領域
の他方から水素を脱着させて前記水素利用装置に供給する水素エネル
ギーシステム。
図3、本発明の実施形態に係る水素吸蔵合金の吸蔵量と水素貯蔵タン
ク内の圧力との関係を示す特性図である。
図4 水素貯蔵タンクの変形例を示す図
図5 水素貯蔵タンクの変形例を示す図
二年魔前、東京工業大学の研究グループが、100 ℃の低温でアンモニア
を合成する鉄触媒の開発し、赤錆を原料とする安価な鉄と水素化バリ
ウム(BaH2)[用語1]の複合材料を触媒とすることで、100 ℃の低温で
水素と窒素からアンモニアを合成に成功している。
(公開日:2023.04.18)
✳️ 関連特許
1️⃣ 特開2024-55069 酸窒化物を触媒担体とするアンモニア分解触媒
国立大学法人東京工業大学
【要約】低い反応温度かつ低い反応圧力でも高いアンモニア分解活性
を有し、かつ大気中、水中に暴露しても反応を繰り返しても触媒活性
の低下が見られないアンモニア分解触媒を提供する。
【解決手段】本発明のアンモニア分解触媒は、担体に遷移金属を担持
したものである。前記担体が、下記一般式(1)で表わされる酸窒化
物である。
AnBmOl-xNy (1)
(前記一般式(1)において、Aは、Ba及びSrからなる群から選
択される少なくとも1種であり、Bは、Ti及びZrからなる群から
選択される少なくとも1種であり、nは、1又は2であり、mは、
1又は2であり、lは、3又は4であり、xは、0.1≦x≦2.0
で表わされる数を表し;yは、0.1≦y≦1.0で表わされる数を
表す。)
【特許請求の範囲】
【請求項1】 担体に遷移金属を担持したアンモニア分解触媒であって、
前記担体が、下記一般式(1)で表わされる酸窒化物である
ことを特徴とするアンモニア分解触媒。
AnBmOl-xNy (1)
(前記一般式(1)において、Aは、Ba及びSrからなる群から選
択される少なくとも1種であり、Bは、Ti及びZrからなる群から
選択される少なくとも1種であり、nは、1又は2であり、mは、1
又は2であり、lは、3又は4であり、xは、0.1≦x≦2.0で
表わされる数を表し;yは、0.1≦y≦1.0で表わされる数を表
す。)
【請求項2】前記遷移金属が、周期表第8族、9族及び10族金属元
素から選ばれる少なくとも1種であることを特徴とする請求項1に記
載のアンモニア分解触媒。
【請求項3】前記遷移金属が、Ru、Fe、Co、Niからなる群か
ら選択される少なくとも1種であることを特徴とする請求項1又は2
に記載のアンモニア分解触媒。
【請求項4】 前記遷移金属が、Niであることを特徴とする請求項
3に記載のアンモニア分解触媒。
【請求項5】 請求項1又は2に記載のアンモニア分解触媒からなる
触媒層に、体積分率0.1~100%のアンモニアガスを連続的に供
給し、0.01MPa~1.0MPaの反応圧力及び300~800
℃の反応温度下、重量空間速度(WHSV)500/mlg-1h-1
以上で接触分解反応させる工程と、を含むことを特徴とする水素の製
造方法。
【発明の効果】【0010】
本発明のアンモニア分解触媒は、低い反応温度かつ低い反応圧力でも
高いアンモニア分解活性を有し、かつ大気中、水中に暴露しても反応
を繰り返しても触媒活性の低下が見られないため、アンモニア分解触
媒として好適である。
【図1】実施例1、比較例1、比較例2におけるアンモニア分解効率
の反応温度依存性を示すグラフである。
【図2】実施例1~3におけるアンモニア分解効率の反応温度依存性
を示すグラフである。
【図3】実施例4における水に対する安定性の評価結果を示すグラフ。
【図4】実施例5及び比較例3における熱に対する安定性の評価結果
を示すグラフ。
【図5】実施例1及び実施例6におけるアンモニア分解効率の反応温
度依存性を示すグラフ。
【図6】実施例1と7、比較例1におけるアンモニア分解効率の反応
温度依存性を示すグラフ。
<アンモニア分解反応>
5質量%Ni/BaTiO3-xNyに代えて、上記得られた 5質量
%Fe/BaTiO3をアンモニア分解触媒として用いて、実施例1
と同じ条件でアンモニア分解反応を実施した。結果を図7に示す。
【図7】実施例1、8、9及び比較例1、4、5におけるアンモニア
分解効率の反応温度依存性
【0155】 「500℃における水素生成速度」
Fe/BaTiO3触媒:0.86mmol/g・h
【0156】【表1】
*反応条件 温度:500℃ 気圧:0.1MPa WHSV:15000
/mlg-1h-1【0157】
【表2】
【0158】(考察)
Ni/BaTiO3-xNy触媒は、Ni/BaTiO3触媒と比較
して、触媒の比表面積やNiの粒子サイズに大きな違いがないにもか
かわらず、非常に大きな活性差がある。Ni/BaTiO3触媒では、
Ni表面が活性点として機能するが、Ni/BaTiO3-xNy触媒
では、BaTiO3-xNy上の窒素空孔サイトが活性点として機能す
るためであると考えられる。以前の研究においても、CaNHのよう
な窒素含有化合物にNiを担持した触媒を用いると、アニオン空孔サ
イトに生じる電子によってアンモニア分子が直接活性化され、低温で
優れたアンモニア分解活性を示すことを明らかにしている(ACS
Catal. 2021、11、11005)。Ni/BaTiO3-
xNy触媒においても同様のメカニズムでアンモニア分子を活性化し
ていると考えられる。一方、Ni/CaNH触媒は、大気中や水中で
は不安定であり、速やかに酸化され触媒活性が大きく低下する。Ni
/BaTiO3-xNy触媒では、安定な酸化物の基本骨格を有するた
め大気安定性、耐水性に優れていると考えられる。
【0159】表1及び表2の結果から分かるように、本実施形態の酸
窒化物を担体として、遷移金属がFe、Coであっても高いアンモニ
ア分解触媒活性を示した。特に、担体として同じBaTiO3-xNy
を用いた場合、Co>Ni>Feの順を示した。
以上
論文情報:
掲載誌 :Journal of the American Chemical Society
論文タイトル :Low-Temperature Ammonia Synthesis on Iron Catalyst
with an Electron Donor
DOI :10.1021/jacs.2c13015
🪄本腰を昨夜から展開している。(その家庭内反動があるが無視、た
だ、体調は無視できず創意工夫)、急遽:電解水素を使用し、アンモニ
ア熱触媒合成法と光触媒炭化水素合成を調査考案をはじめる。「デジ
タル革命渦論」と「ネオコンバーテック創業論」は的中していること
に改めて背筋が締まる思いだ(笑)。これ以外にも分野が異なるが的中
したが(涙)、そこに生成AIがこの成果例を加速させるだろう。東工大
に拍手。 
『ブラームス交響曲第3番 第3楽章 』

今日の言葉:それは『ひ・み・つ』⓶
春が来ても、鳥たちは姿を消し鳴き声も聞こえない。
春だというのに自然は沈黙している。
レイチェル・カーソン 『沈黙の春』